Ο ηλεκτρολύτης είναι ένα ουσιαστικό μέρος μιας μπαταρίας. Χωρίς αυτό το υγρό, απλώς δεν θα λειτουργήσει. Σε αυτό το άρθρο, θα εξηγήσουμε τι είναι, πώς να το προσθέσετε, ποιο θα πρέπει να είναι το ειδικό του βάρος και θα παρέχουμε επίσης μερικούς χρήσιμους πίνακες.
- Ιδιότητες και χαρακτηριστικά ηλεκτρολυτών
- Τι είναι το θειικό οξύ για μια μπαταρία;
- Αποσταγμένο νερό για μπαταρίες
- Προετοιμασία ηλεκτρολύτη για μπαταρίες
- Βασικές ιδιότητες του ηλεκτρολύτη θειικού οξέος
- Ιδιότητα ιξώδους
- Ειδική αντίσταση ηλεκτρολύτη
- Αλκαλικοί ηλεκτρολύτες
- Διάρκεια ζωής ηλεκτρολυτών
- Πώς να ελέγξετε τον ηλεκτρολύτη σε μια μπαταρία αυτοκινήτου;
Ιδιότητες και χαρακτηριστικά ηλεκτρολυτών
Ο ηλεκτρολύτης της μπαταρίας είναι ένα μείγμα απεσταγμένου νερού και θειικού οξέος.
Τι είναι το θειικό οξύ για μια μπαταρία;
Στην εμφάνιση, μοιάζει με μια ελαιώδη ουσία με σημαντικό βάρος. Είναι άοσμο και διαλύεται τέλεια στο νερό. Κατά την παραγωγή ηλεκτρολύτη για μπαταρίες μολύβδου-οξέος, μπορεί να παρατηρηθεί θερμότητα. Αυτό το φαινόμενο είναι υπεύθυνο για τη διάλυση του οξέος.
Οι οδηγοί χρησιμοποιούν το τυπικό οξύ κατηγορίας Α GOST 667-83 για τις μπαταρίες τους. Στα καταστήματα διατίθεται επίσης οξύ υψηλής καθαρότητας, GOST 142b2-78. Συνήθως έχει τα ακόλουθα χαρακτηριστικά:
- Μονοϋδρική 92-94%.
- Πυκνότητα σύμφωνα με το πρότυπο 1,830 g/cm3.
- Ακαθαρσίες έως 0,03665% (σίδηρος 0,012%, οξείδια του αζώτου 0,0001%, μαγγάνιο έως 0,0001%, χλώριο - 0,0005%, αρσενικό - 0,0001%).
Αποσταγμένο νερό για μπαταρίες
Χωρίς αυτό το νερό, είναι απλώς αδύνατο να δημιουργηθεί ένας ηλεκτρολύτης υψηλής ποιότητας. Απαγορεύεται η χρήση H ως υποκατάστατο.2Δεν επιτρέπεται η χρήση νερού από ποτάμι, παροχή νερού ή βρύσης, συμπεριλαμβανομένου του βιομηχανικού και του πόσιμου νερού. Επιτρέπεται το συμπύκνωμα ατμού. Ωστόσο, απαιτείται χημική ανάλυση πριν από τη χρήση. Κατά τη διάρκεια αυτής της διαδικασίας, θα πρέπει να προσδιορίζεται το επίπεδο σιδήρου, το οποίο δεν πρέπει να υπερβαίνει το 0,0004%. Τα επίπεδα χαλκού δεν πρέπει επίσης να υπερβαίνουν το 0,005%.
Οι ηλεκτρονικοί αποστακτήρες χρησιμοποιούνται για την απόκτηση του πολυπόθητου υγρού σε φαρμακεία, εργοστάσια, νοσοκομεία και εργαστήρια. Αυτές οι συσκευές είναι επίσης διαθέσιμες στον μέσο καταναλωτή. Αποσταγμένο νερό μπορεί να ληφθεί χρησιμοποιώντας συσκευές όπως ο αποστακτήρας HR-01, ο αποστακτήρας στήλης Wein, ο Pervach Econom και άλλοι.
Θα πρέπει να ελέγχετε το νερό που παράγεται από τον αποστακτήρα σας κάθε 6 μήνες. Βεβαιωθείτε ότι τα επίπεδα στερεών είναι τα εξής:
- Ασβέστιο – 1,0 mg.
- Αμμωνία – 5 mg ανά λίτρο.
- Θειικά άλατα – έως 0,5 g/l.
- Αμμώνιο όχι περισσότερο από 0,05 mg/l.
- Χλωριούχο όχι μεγαλύτερο από 0,02 mg/l.
Επιπλέον, το απεσταγμένο νερό θα πρέπει να ελέγχεται για νιτρικά άλατα, σίδηρο και βαρέα μέταλλα. Ο πίνακας που προκύπτει θα πρέπει να αναφέρει εάν αυτό το νερό μπορεί να χρησιμοποιηθεί για τη δημιουργία ηλεκτρολυτών. Πρέπει να συμμορφώνεται με το GOST 6709-72.
Σε κανονικά καταστήματα λιανικής πώλησης, ένα μπουκάλι νερό 1,5 λίτρων μπορεί να αγοραστεί για 20-30 ρούβλια.
Προετοιμασία ηλεκτρολύτη για μπαταρίες
Ο ηλεκτρολύτης της μπαταρίας είναι ουσιαστικά ένα υδατικό διάλυμα H2ΕΤΣΙ4Χρησιμοποιήστε νερό και οξύ με τις παραμέτρους που περιγράφονται παραπάνω. Για την πλήρωση και τη συμπλήρωση, χρησιμοποιήστε ηλεκτρολύτη με πυκνότητα 1,18-1,24 g/cm³. Μπορεί να χρησιμοποιείτε πυκνότητα 1,83 g/cm³.3 στη συνέχεια, χωρίστε τη διαδικασία σε δύο προσεγγίσεις:
- Αρχικά, δημιουργήστε έναν ηλεκτρολύτη 1,4 g/cm3Περιμένετε μέχρι η θερμοκρασία του να πέσει στους 20 βαθμούς Κελσίου.
- Στη συνέχεια, παρασκευάστε τον απαιτούμενο ηλεκτρολύτη από αυτόν τον ηλεκτρολύτη.
Αυτή η προσέγγιση θα αποτρέψει την υπερβολική θέρμανση του θειικού οξέος.
Ο ηλεκτρολύτης πρέπει να παρασκευάζεται σε ειδικό δοχείο. Αυτό μπορεί να είναι πλαστικό, πήλινο ή εβονίτης. Μόλυβδος ικανότηταΑυτό θα λειτουργήσει επίσης. Αλλά ποτέ μην χρησιμοποιείτε γυάλινο μπολ. Θα ραγίσει λόγω των υψηλών θερμοκρασιών.
Το πρώτο πράγμα που πρέπει να κάνετε είναι να ρίξετε μια ορισμένη ποσότητα απεσταγμένου H2Ο. Μετά από αυτό, ρίξτε την απαιτούμενη ποσότητα θειικού οξέος σε λεπτό ρεύμα. Ανακατέψτε το μείγμα συνεχώς με μια γυάλινη ράβδο. Είναι καλύτερο εάν το H2ΕΤΣΙ4 Θα το προσθέσετε σε δόσεις.
Να ρίχνετε πάντα οξύ στο νερό. Διαφορετικά, θα καταλήξετε με ένα κοκτέιλ από επικίνδυνα σταγονίδια οξέος που θα πετάνε προς όλες τις κατευθύνσεις. Αυτό θα μπορούσε να προκαλέσει εγκαύματα στο σώμα σας και να προκαλέσει ζημιά σε κοντινά αντικείμενα.
Προστατευτικός εξοπλισμός για την εργασία:
- Λαστιχένιες μπότες.
- Γάντια κατασκευασμένα από το ίδιο υλικό.
- Ειδικές υφασμάτινες φόρμες.
- Γυαλιά για προστασία.
- Ποδιά με επένδυση από καουτσούκ.
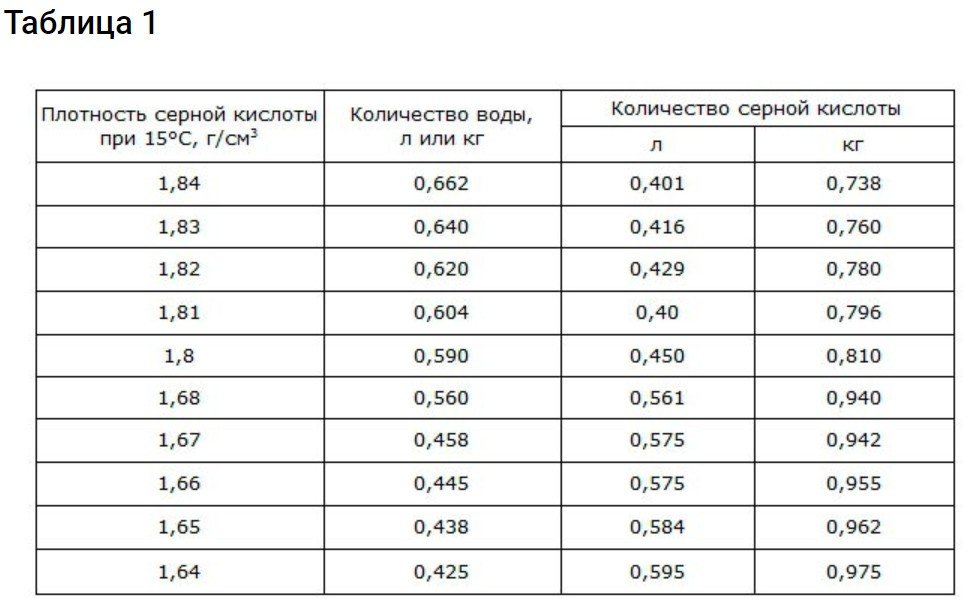
Παρακάτω θα βρείτε ειδικούς πίνακες από τους οποίους μπορείτε να καταλάβετε ποιες αναλογίες πρέπει να τηρούνται.
Δεδομένα σχετικά με την αναλογία θειικού οξέος προς απεσταγμένο νερό
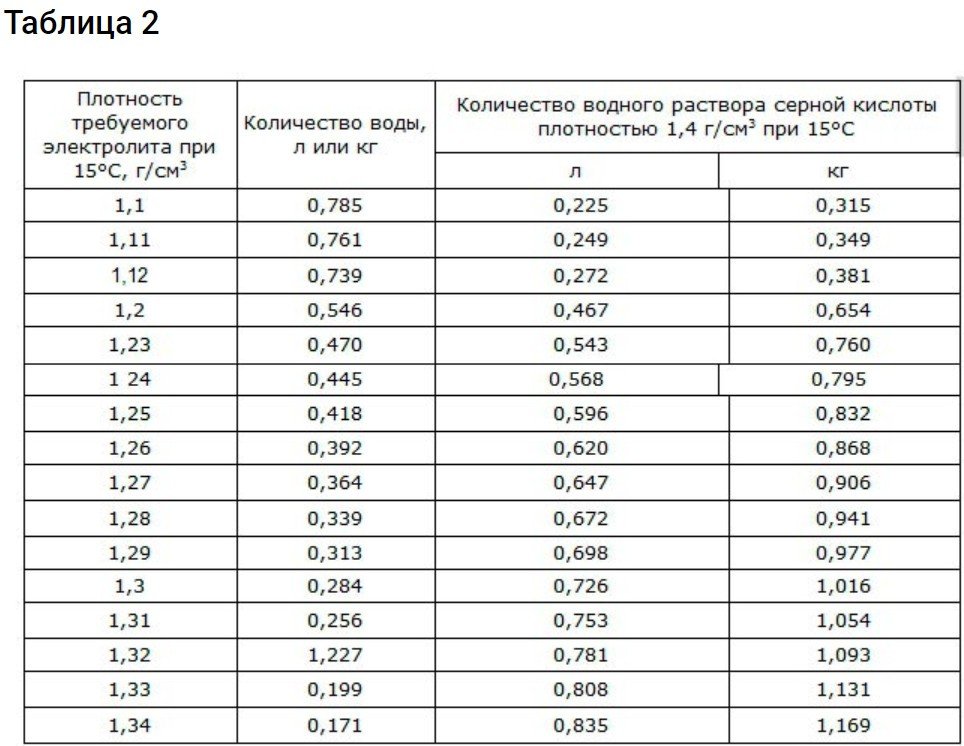
Για να επιτευχθεί πυκνότητα 1,4 g/cm3 Πρέπει να τηρήσετε τα δεδομένα από τον 2ο πίνακα.
Για να επιτευχθεί πυκνότητα 1,83 g/cm3 Χρησιμοποιήστε τις πληροφορίες που παρέχονται παρακάτω.
Για τη λήψη πληροφοριών πυκνότητας θα πρέπει να χρησιμοποιείται υδρόμετρο. Κατά τη μέτρηση της θερμοκρασίας, το θερμόμετρο δεν πρέπει να περιέχει ξύλο ή μέταλλο. Οι μετρήσεις θα πρέπει να λαμβάνονται όταν η θερμοκρασία πέσει στους 20 βαθμούς.
Η κλίση θερμοκρασίας-πυκνότητας αντιστοιχεί σε μια τιμή 0,0007 g/cm³ ανά 1°C. Εάν η θερμοκρασία είναι πάνω από 20°C, μια διόρθωση στους υπολογισμούς προστίθεται στα μετρούμενα δεδομένα πυκνότητας. Ας υποθέσουμε ότι η πραγματική θερμοκρασία είναι 30°C και η δική μας είναι 20°C. Τότε η διαφορά θα είναι 10°C.0Λοιπόν, να τι παίρνουμε: 0,0007 x 10 = 0,07 g/cm3. Δηλαδή, προσθέτουμε ένα σφάλμα 0,007 g/cm3 στα δεδομένα πυκνότητας που λάβαμε.
Εάν η πραγματική θερμοκρασία είναι 10 βαθμοί, η διαφορά με την παραπάνω θερμοκρασία θα είναι 10 βαθμοί Κελσίου.00,0007 g/cm3 πολλαπλασιάζεται επί δέκα και η διόρθωση είναι 0,007 g/cm3. Σε αυτήν την περίπτωση, η διόρθωση αφαιρείται από τη μετρούμενη πυκνότητα στους t = 10°C.0.
Απαγορεύεται η συμπλήρωση του ηλεκτρολύτη περισσότερο από 25 ντο0.
Βασικές ιδιότητες του ηλεκτρολύτη θειικού οξέος
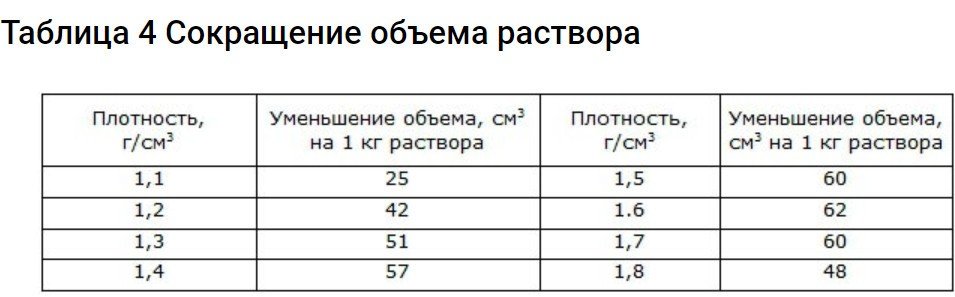
Εκτός από τα παραπάνω, θα πρέπει να ληφθεί υπόψη ένας ακόμη παράγοντας. Εάν λάβετε τον ίδιο όγκο οξέος και νερού, ο όγκος που προκύπτει μετά την ανάμειξη θα είναι σημαντικά μικρότερος. Επομένως, αυτή η παράμετρος πρέπει επίσης να λαμβάνεται υπόψη κατά την παρασκευή του ηλεκτρολύτη. Για να το κάνετε αυτό, χρησιμοποιήστε τα δεδομένα στον πίνακα.
Ιδιότητα ιξώδους
Επηρεάζει την απόδοση των μπαταριών με πλάκες μολύβδου. Η διαδικασία στις μπαταρίες είναι διάχυση. Ο ρυθμός αυτής της διάχυσης εξαρτάται από το ιξώδες. Αυτό το ιξώδες καθορίζει πόσο γρήγορα ο ηλεκτρολύτης φτάνει στην επιφάνεια και τους πόρους των ηλεκτροδίων κατά την εκφόρτιση.
Εάν το ιξώδες αυξηθεί, η διάχυση θα επιβραδυνθεί. Όταν η θερμοκρασία πέσει κατά 25 βαθμούς, το ιξώδες διπλασιάζεται. Στους 50°C0 η αύξησή του συμβαίνει 30 φορές σε σύγκριση με το κανονικό t.
Όταν το ιξώδες αυξάνεται, τότε χωρητικότητα μπαταρίαςμειώνεται. Εξαιτίας αυτού, η απόδοση των μπαταριών μολύβδου-οξέος σε κρύο καιρό μειώνεται. Αυτό πρέπει να λαμβάνεται υπόψη κατά την εγκατάσταση μπαταρίες τζελ.
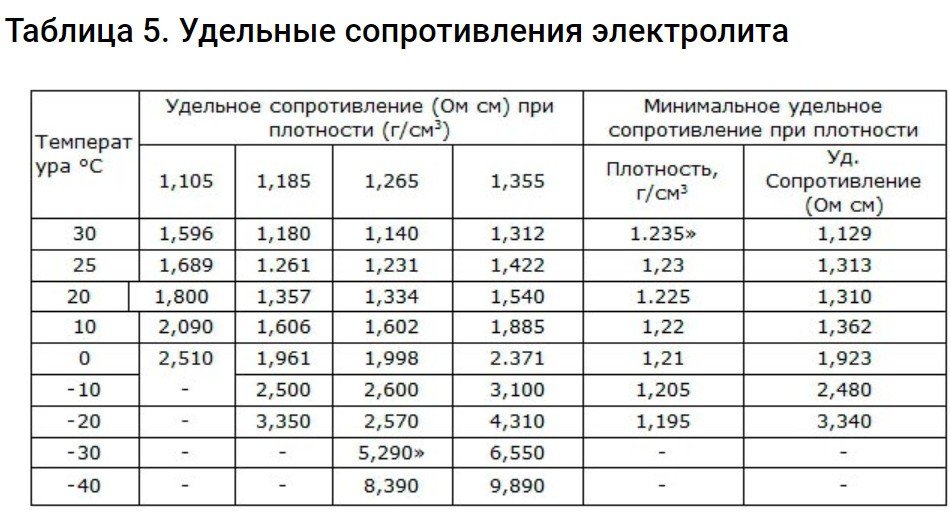
Ειδική αντίσταση ηλεκτρολύτη
Για να το υπολογίσετε, θα πρέπει να καταφύγετε στον τύπο =rS/L. Είναι σημαντικό όταν η αντίσταση του ηλεκτρολύτη που καταλαμβάνει ικανότητα, περιορίζεται σε μήκος 1 εκατοστό και διατομή 1 cm3Η σημασία των γραμμάτων στον τύπο:
- L – μήκος.
- r – ειδική αντίσταση σε ohms cm.
- S – διατομή cm2.
Το R αλλάζει τη στιγμή που αλλάζει η θερμοκρασία και η συγκέντρωση του ηλεκτρολύτη. εσωτερική αντίστασηΕάν η μπαταρία είναι μικρή, θα πρέπει να χρησιμοποιήσετε έναν ηλεκτρολύτη με το χαμηλότερο ειδικό R.
Οι παράμετροι τέτοιων αντιστάσεων βρίσκονται σε αυτόν τον πίνακα.
Το R αυξάνεται καθώς μειώνεται η θερμοκρασία, ειδικά κάτω από το μηδέν βαθμούς.
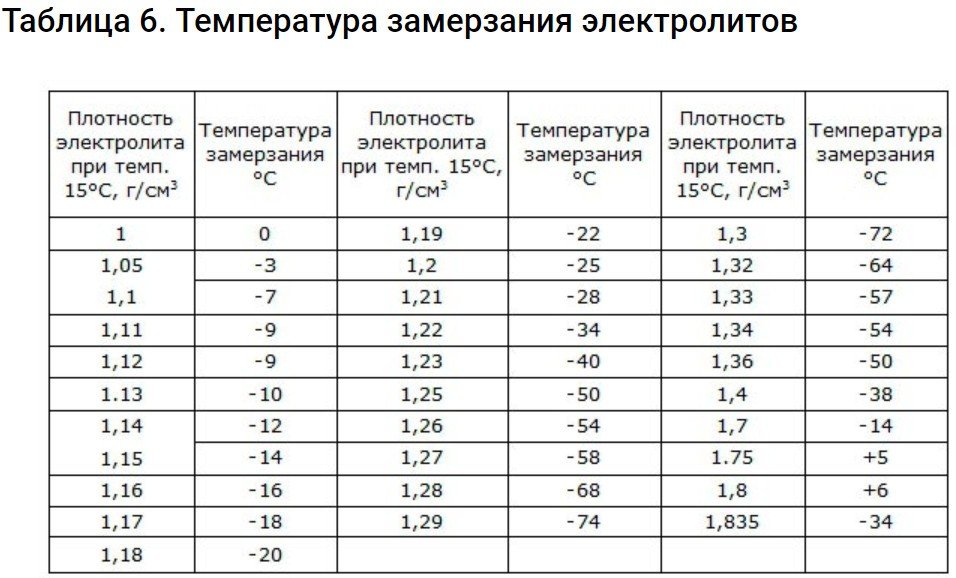
Στην πραγματικότητα, το σημείο πήξης του ηλεκτρολύτη είναι ένας σημαντικός δείκτης. Καθώς η μπαταρία αποφορτίζεται, η πυκνότητα και το σημείο πήξης της μειώνονται. Σε χαμηλές θερμοκρασίες, ο όγκος του υγρού αυξάνεται, οδηγώντας σε ζημιά στα ηλεκτρόδια και στην ίδια την μπαταρία.
Ηλεκτρολύτης με πυκνότητα 1,29 g/cm3 έχει το χαμηλότερο σημείο πήξης.
Οι μπαταρίες εκκίνησης που χρησιμοποιούνται σε ψυχρές συνθήκες έχουν πυκνότητα 1,26-1,30 g/cm2Αυτός ο ηλεκτρολύτης δεν παγώνει ακόμη και στον πιο κρύο καιρό.
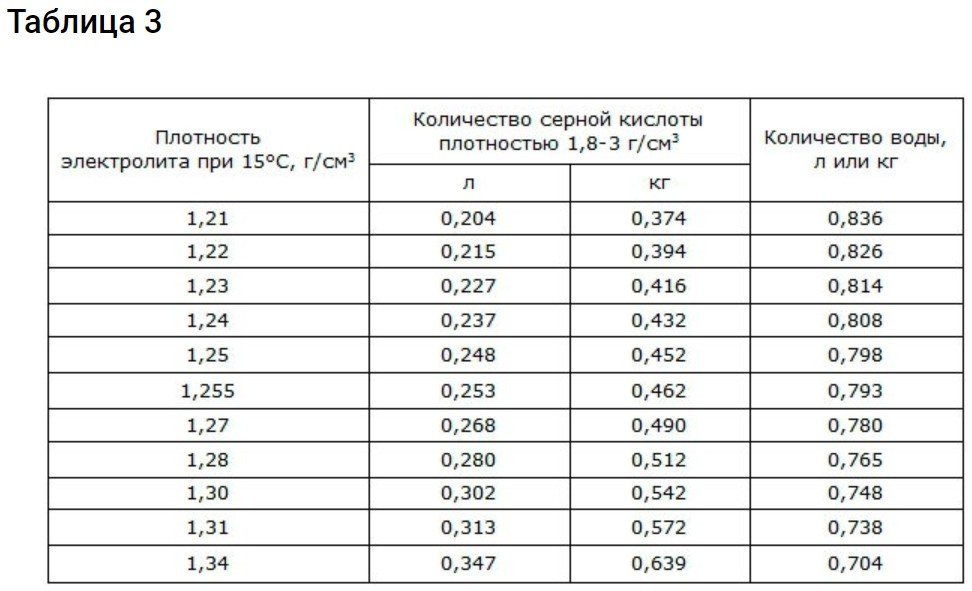
Ο παρακάτω πίνακας δείχνει τα επίπεδα πυκνότητας στα οποία συμβαίνει η κατάψυξη.
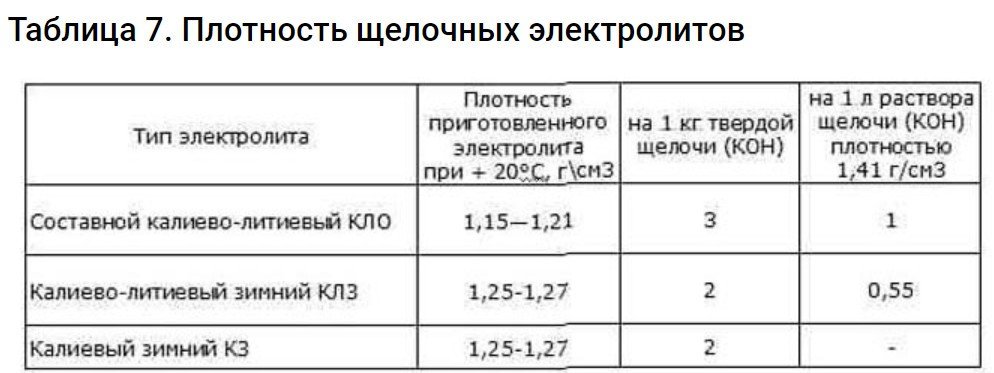
Αλκαλικοί ηλεκτρολύτες
Για την παρασκευή τους χρησιμοποιούνται λίθιο και κάλιο· και τα δύο είναι καυστικά.
Η καυστική ποτάσα, ή KOH εν συντομία, είναι λευκή, στερεή και ιδιαίτερα διαλυτή στο H2.2Α. Όταν διαλύεται, απελευθερώνεται θερμότητα. Σύμφωνα με το πρότυπο GOST, η ουσία αυτή παράγεται σε τέσσερις ποιότητες:
- Υψηλότερα.
- ΕΝΑ
- Τύπος Β.
- Πίδακας.
Η πρώτη κατηγορία περιέχει έως και 96% καυστικό κάλιο. Η δεύτερη κατηγορία, "Α", περιέχει έως και 92%. Η τρίτη κατηγορία, "Β", περιέχει 88%. Η τέταρτη κατηγορία έχει λιγότερες ακαθαρσίες από την τεχνική κατηγορία.
Όταν δημιουργείτε έναν ηλεκτρολύτη από λίθιο και κάλιο, πρώτα διαλύστε το κάλιο και στη συνέχεια προσθέστε το λίθιο. Αυτό γίνεται με ρυθμό 10-20 γραμμαρίων ανά 1 λίτρο ηλεκτρολύτη. Στη συνέχεια, αφήστε το να καθίσει για 15-20 ώρες. Αυτό επιτρέπει στην θερμοκρασία να πέσει και στις ακαθαρσίες να καθιζάνουν. Πριν αφήσετε το διάλυμα, καλύψτε το καλά με ένα καπάκι.
Το προκύπτον υγρό διάλυμα θα πρέπει στη συνέχεια να χυθεί σε ένα καθαρό δοχείο. Στη συνέχεια, ελέγξτε το ειδικό βάρος με ένα υδρόμετρο. Εάν είναι απαραίτητο, ρυθμίστε το ειδικό βάρος στο σωστό επίπεδο. Στη συνέχεια, προσθέστε αλκάλια και νερό. Εναλλακτικά, μπορείτε να προσθέσετε έναν έτοιμο συμπυκνωμένο ηλεκτρολύτη.
Τι πυκνότητα απαιτεί η μπαταρία σας; Αυτές οι πληροφορίες βρίσκονται στην τεχνική της τεκμηρίωση. Εάν η τεκμηρίωση δεν περιέχει κρίσιμες συστάσεις, τότε μπορεί να χρησιμοποιηθεί ηλεκτρολύτης 1,19-1,21 g/cm3.3 στους 15 βαθμούς Κελσίου. Θα πρέπει επίσης να περιέχει 10-20 g/l Li.
Είναι σημαντικό να σημειωθεί ότι ένα υγρό με αυτά τα χαρακτηριστικά χρησιμοποιείται καλύτερα σε θερμοκρασίες όχι χαμηλότερες από 20 βαθμούς Κελσίου. Σε χαμηλότερες θερμοκρασίες, είναι κατάλληλη πυκνότητα 1,25–1,27 g/cm3.3Αλλά χωρίς τη χρήση καυστικού λιθίου.
Για την αναζωογόνηση των μπαταριών σιδήρου-νικελίου και αλκαλικών μπαταριών καδμίου-νικελίου, χρησιμοποιείται ένας ηλεκτρολύτης με βάση το λίθιο και το κάλιο με πυκνότητα 1,255-1,279 g/cm3.3Σε όλα αυτά, πρέπει να προσθέσετε 69 γραμμάρια καυστικού λιθίου ανά 1 λίτρο ηλεκτρολύτη.
Για ευκολία στην προετοιμασία, χρησιμοποιήστε τον πίνακα.
Διάρκεια ζωής ηλεκτρολυτών
Μπορεί να αποθηκευτεί επ' αόριστον. Για να αποφύγετε τις βροχοπτώσεις, φυλάξτε το μακριά από το άμεσο ηλιακό φως. Επίσης, αποφύγετε τις διακυμάνσεις της θερμοκρασίας. Η πραγματική διάρκεια ζωής του ηλεκτρολύτη της μπαταρίας είναι άγνωστη, καθώς επηρεάζεται από πολλούς παράγοντες.
Πώς να ελέγξετε τον ηλεκτρολύτη σε μια μπαταρία αυτοκινήτου;
Ο έλεγχος θα πρέπει να πραγματοποιείται δύο φορές κάθε 12 μήνες: πριν από τον χειμώνα και στις αρχές του καλοκαιριού.
Εργαλεία για την εκτέλεση αυτής της διαδικασίας:
- Υδρόμετρο – σας επιτρέπει να μετρήσετε την πυκνότητα.
- Γυάλινος σωλήνας με διάμετρο 5-7 mm.
Αλγόριθμος επαλήθευσης:
- Αφαιρέστε την μπαταρία από το αυτοκίνητο.
- Ξεβιδώστε όλα τα βύσματα.
- Τοποθετήστε το υδρόμετρο με το άκρο εργασίας σε ένα τμήμα.
- Χρησιμοποιώντας τη λάμπα της συσκευής, τραβήξτε τον ηλεκτρολύτη μέχρι ο πλωτήρας να ανέβει και να αρχίσει να επιπλέει χωρίς να αγγίζει τα τοιχώματα του υδρόμετρου.
- Η πυκνότητα μπορεί να παρατηρηθεί στο σημείο όπου η ράβδος και ο ηλεκτρολύτης αγγίζουν το ένα το άλλο.
- Καταγράψτε τις πληροφορίες που λάβατε σε ένα φύλλο χαρτιού.
Μια παρόμοια διαδικασία θα πρέπει να επαναληφθεί με κάθε συστοιχία μπαταριών.
Λίγοι άνθρωποι χρησιμοποιούν αυτοσχέδιο ηλεκτρολύτη μπαταρίας στις μέρες μας. Απλώς επισκεφθείτε οποιοδήποτε κατάστημα και αγοράστε την απαραίτητη ουσία με μια μικρή χρέωση. Αυτό θα σας εξοικονομήσει χρόνο και θα προστατεύσει τη ζωή σας!