Το πρώτο γαλβανικό στοιχείο στον κόσμο αναπτύχθηκε από τον Luigi Galvani. Διαβάστε για την ιστορία του. σε αυτό το άρθροΟυσιαστικά, είναι μια προσωρινή πηγή ηλεκτρικού ρεύματος που παράγεται από μια χημική αντίδραση. Η ροή ηλεκτρονίων παράγεται από την αλληλεπίδραση μεταξύ δύο ανόμοιων μετάλλων. Ως αποτέλεσμα, η χημική ενέργεια μετατρέπεται σε ηλεκτρική ενέργεια, η οποία στη συνέχεια μπορεί να χρησιμοποιηθεί στην καθημερινή ζωή.
Ένα γαλβανικό στοιχείο συγκέντρωσης είναι μια πηγή ρεύματος που αποτελείται από δύο πανομοιότυπα μεταλλικά ηλεκτρόδια τοποθετημένα σε ένα μείγμα αλάτων αυτού του μετάλλου σε διάφορες συγκεντρώσεις.
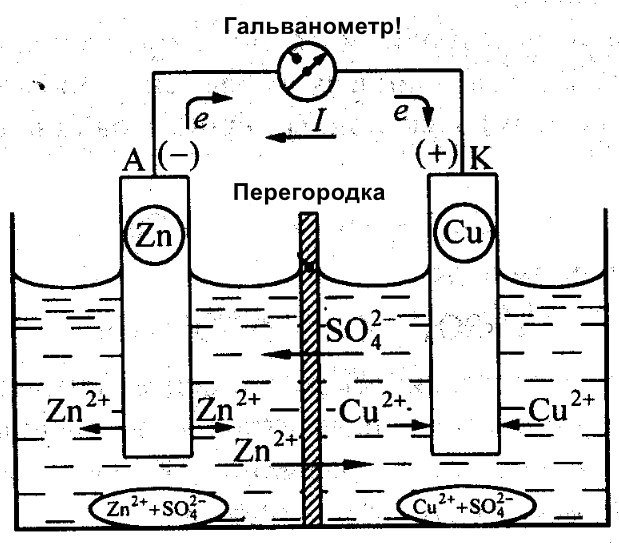
Εκτός από τον Galvani, ο Daniel Jacobi εργάστηκε επίσης στη δημιουργία μιας αποδοτικής μπαταρίας. Τροποποίησε ελαφρώς την πηγή ενέργειας που δημιούργησε. Αποτελείται από μια πλάκα χαλκού τοποθετημένη σε CuSO4 και μια πλάκα ψευδαργύρου βυθισμένη σε ZnSO4. Για να αποτραπεί η άμεση αλληλεπίδρασή τους, τοποθετείται ένα πορώδες τοίχωμα ανάμεσά τους. Παρακάτω είναι ένα διάγραμμα του γαλβανικού στοιχείου του Daniel Jacobi.
Ο ψευδάργυρος και ο χαλκός έχουν διαφορετική αντιδραστικότητα και επομένως το φορτίο τους θα διαφέρει. Ως αποτέλεσμα, τα επίπεδα των ηλεκτροδίων δεν είναι επίσης ομοιόμορφα. Αυτό τους επιτρέπει να κινούνται και να παράγουν ηλεκτρικό ή γαλβανικό ρεύμα. Αυτό το ρεύμα αρχίζει να ρέει όταν ένα άτομο ή ο εφευρέτης μιας συσκευής αποθήκευσης ρεύματος συνδέει ένα φορτίο. Αυτό το φορτίο θα μπορούσε να είναι μια λάμπα, ένα ραδιόφωνο, ένα ποντίκι υπολογιστή ή άλλες ηλεκτρικές συσκευές.
Σχηματικό διάγραμμα ενός γαλβανικού στοιχείου
Ένα διάγραμμα κυκλώματος αναφέρεται στη σύνθεση και τη δομή του. Μπορεί να κατασκευαστεί από διάφορα χημικά στοιχεία χρησιμοποιώντας βοηθητικές συσκευές. Παρακάτω, θα περιγραφεί συνοπτικά η δομή ενός γαλβανικού στοιχείου. Διαβάστε περισσότερα σχετικά με αυτό σε αυτό το άρθρο.!
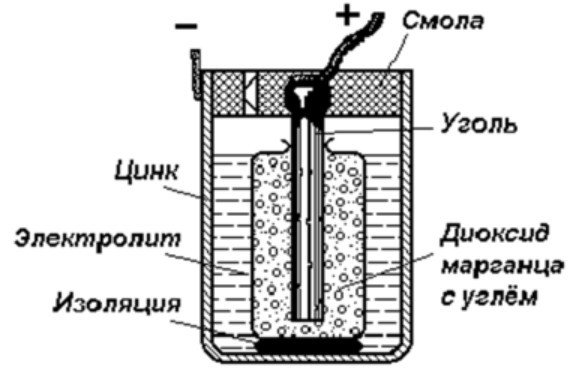
Η δομή ενός γαλβανικού στοιχείου
Η απλούστερη συσκευή αποθήκευσης ενέργειας αποτελείται από:
- Ράβδος άνθρακα.
- Δύο ανόμοια μέταλλα.
- Ηλεκτρολύτης.
- Ρητίνη ή πλαστικό.
- Απομονωτής.
Όπως φαίνεται από αυτό το διάγραμμα, ένα γαλβανικό στοιχείο αποτελείται από ένα αρνητικό και ένα θετικό ηλεκτρόδιο. Μπορούν να κατασκευαστούν από χαλκό, ψευδάργυρο ή άλλα μέταλλα. Ονομάζονται στοιχεία χαλκού-ψευδαργύρου. Μερικές φορές ονομάζονται ξηρές μπαταρίες.
Ονομασία ενός γαλβανικού στοιχείου σε ένα διάγραμμα Είναι κατασκευασμένο με τη μορφή δύο κάθετων γραμμών, κοντά η μία στην άλλη σε μικρή απόσταση. Η μία από αυτές θα είναι μικρότερη. Στις άκρες κάθε τέτοιας γραμμής υπάρχουν πινακίδες που υποδεικνύουν πόλωσηΗ μακριά γραμμή σημειώνεται θετικά και η κοντή γραμμή αρνητικά. Η τάση μπορεί να εμφανίζεται δίπλα της. Αυτό σημαίνει ότι το κύκλωμα που χρησιμοποιεί την μπαταρία λειτουργεί μόνο σε αυτήν την τάση.
Η αρχή λειτουργίας ενός γαλβανικού στοιχείου
Ένα γαλβανικό στοιχείο λειτουργεί μέσω της κίνησης ηλεκτρονίων από τη μία μεταλλική επαφή στην άλλη. Πραγματοποιείται ένας χημικός μετασχηματισμός. Διαβάστε περισσότερα για τη θερμοδυναμική ενός γαλβανικού στοιχείου και τον σχηματισμό του γαλβανικού ηλεκτρισμού. Εδώ.
Απαντήσεις σε συχνές ερωτήσεις
| Γαλβανικός | Εξήγηση |
| Μπαταρία | Μια πηγή ενέργειας που λειτουργεί μέσω διεργασιών που λαμβάνουν χώρα σε έναν περιορισμένο, μικροσκοπικό χώρο. Συγκεκριμένα, η ενέργεια παράγεται μέσω μιας χημικής αντίδρασης. |
| Βολταϊκό κύτταρο ή βολταϊκός σωρός | Αυτό είναι ένα ενεργειακό στοιχείο που δημιουργήθηκε για πρώτη φορά από έναν επιστήμονα ονόματι Βολτ. |
| Διαδικασία | Η αλληλεπίδραση μεταξύ χημικών στοιχείων που έχει ως αποτέλεσμα τον σχηματισμό ηλεκτρικού ρεύματος. |
| Εκπλήρωση | Αυτή είναι η ολοκλήρωση μιας χημικής αντίδρασης. Δηλαδή, δεν θα υπάρχει αλληλεπίδραση μεταξύ των ουσιών. Η γαλβανική εκκένωση υπάρχει στο Warframe. Ουσιαστικά, είναι μια τροποποίηση που είναι σε έλλειψη. Χρησιμοποιείται για όπλα μάχης σώμα με σώμα. ΠόλωσηΈκδοση 2. |
| Γαλβανική επαφή | Αυτή είναι η επαφή μεταξύ των ηλεκτροδίων και του διαλύματος. |
| Αποτέλεσμα | Η εμφάνιση μιας διαφοράς μεταξύ δύο επαφών κατασκευασμένων από δύο είδη μετάλλου. Το μέγεθος εξαρτάται από τη θερμοκρασία και τη χημεία των αγωγών. Ουσιαστικά, αυτός είναι ο πρώτος νόμος του Βόλτα. |
| Σύνδεση/κρίκος/αλυσίδα | Σύνδεση δύο ή περισσότερων τμημάτων ενός ηλεκτρικού κυκλώματος σε μια πηγή ρεύματος. |
| Γαλβανικό φορτίο | Γεμίζοντας την μπαταρία με ενέργεια. |
Ο γαλβανισμός είναι μια χημική διαδικασία που χρησιμοποιεί ηλεκτρικό ρεύμα. Η αντίδραση μειώνει την ποσότητα των διαλυμένων μεταλλικών κατιόντων σε τέτοιο βαθμό που τελικά σχηματίζουν μια ομοιόμορφη επικάλυψη σε ένα μεταλλικό ηλεκτρόδιο. Ως αποτέλεσμα, το αντικείμενο γίνεται πιο ανθεκτικό, τα μικρά βαθουλώματα εξαφανίζονται και η εμφάνισή του γίνεται πιο ελκυστική.
Τύποι γαλβανικών στοιχείων
Υπάρχουν διάφοροι συγκεκριμένοι τύποι μπαταριών.
Πίνακας γαλβανικών στοιχείων
| Τύπος | Δυναμικό | Κύρια πλεονεκτήματα |
| Λίθιο | 3 V | Μεγάλος ικανότητα, υψηλό ρεύμα. |
| Μπαταρίες αλατιού ή άνθρακα-ψευδάργυρο | 1,5 ίντσα | Το φθηνότερο. |
| Νικέλιο οξυυδροξυλίου NiOOH | 1,6 βολτ | Υψηλό ρεύμα. Υψηλή χωρητικότητα. |
| Αλκαλικό ή αλκαλικό | 1,6 V | Υψηλό ρεύμα. Καλή ένταση. |
Αυτό το θέμα καλύπτεται με περισσότερες λεπτομέρειες στο άρθρο. είδη μπαταριών!
Σκοπός ενός γαλβανικού στοιχείου
Έχει σχεδιαστεί για την εκκίνηση ηλεκτρικού εξοπλισμού. Αυτά μπορεί να περιλαμβάνουν:
- Ρολόι.
- Τηλεχειριστήρια.
- Φακοί.
- Ιατρικός εξοπλισμός.
- Φορητοί υπολογιστές.
- Παιχνίδια.
- Μπρελόκ.
- Τηλέφωνα.
- Δείκτες λέιζερ.
- Αριθμομηχανές.
Και παρόμοια πράγματα γύρω μας.
Γαλβανικό στοιχείο στο σπίτι
Μπορείτε να φτιάξετε μόνοι σας μια απλή πηγή ενέργειας. Για να το κάνετε αυτό, θα χρειαστείτε τα ακόλουθα υλικά:
- Πλαστικό κύπελλο.
- Ηλεκτρολύτης. Αυτό μπορεί να είναι ένα αλατούχο διάλυμα, σόδα ή κιτρικό οξύ αραιωμένο σε νερό.
- Πλάκες από δύο διαφορετικά μέταλλα. Για παράδειγμα, αλουμίνιο και χαλκός.
- Σύρματα
Διαδικασία κατασκευής
Πάρτε ένα πλαστικό ποτήρι και ρίξτε μέσα τον ηλεκτρολύτη. Μην το γεμίσετε μέχρι το χείλος. Είναι καλύτερο να το αφήσετε 1-2 εκατοστά κοντά. Συνδέστε τα καλώδια στις μεταλλικές πλάκες. Στη συνέχεια, τοποθετήστε τις πλάκες χαλκού και αλουμινίου στις άκρες του δοχείου. Θα πρέπει να είναι παράλληλες μεταξύ τους. Μόλις όλα είναι έτοιμα, μπορείτε να μετρήσετε την τάση με ένα βολτόμετρο.
Συνδέστε τη συσκευή και αγγίξτε τους αισθητήρες στις επαφές της πηγής τροφοδοσίας μας. Κρατήστε τους στη θέση τους μέχρι να εμφανιστεί η τάση στην οθόνη. Συνήθως, είναι 0,5-0,7 βολτ. Αυτές οι τιμές εξαρτώνται από τον ηλεκτρολύτη ή, πιο συγκεκριμένα, από την ουσία που χρησιμοποιείται ως ηλεκτρολύτης.
Έτσι κατασκευάζεται ένα αυτοσχέδιο γαλβανικό στοιχείο.